آموزش پلی آمیدها در شیمی یازدهم: سفر از متیل آمین تا کولار ضدگلوله

پلیآمیدها یکی از جذابترین و کاربردیترین مباحث درسی هستند که به عنوان بخشی از فصل سوم شیمی یازدهم باید مطالعه کنید. این ترکیبات شیمیایی نقش بسیار مهمی هم در بدن موجودات زنده و هم در صنایع پیشرفته امروزی ایفا میکنند. درک صحیح این مبحث نه تنها در موفقیت تحصیلی، بلکه در شناخت دنیای اطراف ما نیز تأثیر مستقیم دارد.
در این مقاله آموزشی از سایت تدریس شیمی متین هوشیار، به طور کامل و ساختاریافته به بررسی پلیآمیدها میپردازیم. از شناخت ساختار مولکولی و گروه عاملی آمید شروع میکنیم و تا کاربردهای شگفتانگیز پلیآمیدهای مصنوعی مانند کولار پیش میرویم. تمامی مطالب بر اساس آخرین استانداردهای آموزشی و متناسب با نیازهای دانشآموزان پایه یازدهم تدوین شده است.
هدف از این آموزش، ارائه یک مرجع کامل و در عین حال قابل فهم است که بتواند به سؤالات متداول دانشآموزان پاسخ دهد. مطالب به گونهای تنظیم شده که علاوه بر پوشش کامل مفاهیم درسی، بینش بهتری نسبت به کاربردهای عملی شیمی در زندگی روزمره ایجاد کند. این مقاله به شما کمک میکند تا به صورت مفهومی و پایهای بر این مبحث مسلط شوید.
پلی آمیدهای طبیعی؛ قهرمانان گمنام بدن ما
پلی آمیدها فقط محصول آزمایشگاههای شیمی نیستند. طبیعت سالهاست که این پلیمرهای هوشمند را میسازد و از آنها برای ایجاد قویترین و انعطافپذیرترین ساختارها استفاده میکند. این پلیمرهای طبیعی در ساختار خود اتمهای کربن، هیدروژن، اکسیژن و نیتروژن دارند. نقطه مشترک همه آنها، وجود گروه عاملی آمید است که مانند یک ستون محکم، زنجیرههای پلیمری را به هم متصل میکند. درک این پلیمرهای طبیعی، کلید فهمیدن پلی آمیدهای مصنوعی است.
بدن انسان یک کارخانه شیمیایی شگفتانگیز است که از پلی آمیدها برای ساخت اجزای حیاتی خود استفاده میکند. این مواد طبیعی برخلاف ظاهرشان، استحکام فوقالعادهای دارند. آنها میتوانند در برابر فشار، کشش و سایش مقاومت کنند. این دوام بالا دلیل محکم بودن موها و ناخنهای ماست. طبیعت با استفاده از این پلیمرها، بهینهترین طراحی ممکن را برای موجودات زنده انجام داده است.
حیوانات نیز از این قاعده مستثنی نیستند. پلی آمیدهای طبیعی نقش حفاظتی و پشتیبانی بسیار مهمی برای آنها ایفا میکنند. این پلیمرها به صورت الیاف بسیار باریک و مستحکم ساخته میشوند. سپس این الیاف در کنار هم قرار میگیرند و ساختارهای بزرگتر را تشکیل میدهند. این فرآیند هوشمندانه طبیعت، منجر به ایجاد موادی میشود که هم سبک هستند و هم مقاومت خارقالعادهای دارند.
گروه عاملی آمید؛ ستون فقرات پلی آمیدها
گروه عاملی آمید قلب تپنده تمام پلی آمیدها، چه طبیعی و چه مصنوعی، است. این گروه از پیوند یک اتم نیتروژن با یک گروه کربونیل (C=O) تشکیل شده است. این آرایش اتمی خاص، به گروه آمید خواص فیزیکی و شیمیایی منحصر به فردی میدهد. پیوندهای هیدروژنی قوی که این گروهها میتوانند با یکدیگر تشکیل دهند، دلیل اصلی استحکام بالای پلی آمیدهاست.
این گروه عاملی از طریق یک واکنش شیمیایی بسیار مهم به نام «واکنش تراکمی» تشکیل میشود. در این واکنش، یک گروه کربوکسیلیک اسید (COOH) با یک گروه آمین (NH₂) برهمکنش میدهد. نتیجه این برهمکنش، تشکیل پیوند آمیدی و آزاد شدن یک مولکول آب است. این فرآیند پایه و اساس تشکیل تمام پلیمرهای آمیدی است.
تکرار زنجیرهای این گروه عاملی است که یک پلیمر را به وجود میآورد. زمانی که صدها یا هزاران گروه آمید در یک زنجیره طولانی کنار هم قرار میگیرند، یک پلی آمید تشکیل میشود. استحکام نهایی پلیمر به طول این زنجیره و تعداد پیوندهای هیدروژنی بین زنجیرهها بستگی دارد. هرچه این پیوندها بیشتر باشند، پلیمر محکمتر خواهد بود.
نمونههایی از پلی آمیدهای طبیعی در اطراف ما
پلی آمیدهای طبیعی آنقدر در زندگی روزمره ما فراوان هستند که اغلب به سادگی از کنار آنها عبور میکنیم. کراتین، یک پلی آمید بسیار رایج، ماده اصلی تشکیلدهنده مو، ناخن، پوست و پشم است. این پروتئین ساختاری، استحکام و انعطافپذیری لازم را به این بافتها میدهد. موی انسان یکی از قویترین الیاف طبیعی شناخته شده است.
حیوانات نیز به شدت به این پلیمرهای طبیعی وابسته هستند. شاخ کرگدن و سم گاو نمونههای بارزی از پلی آمیدهای طبیعی با استحکام بسیار بالا هستند. پشم گوسفند که از کراتین ساخته شده، یک عایق حرارتی طبیعی و بسیار کارآمد است. این ماده نه تنها گرما را حفظ میکند، بلکه در برابر رطوبت نیز مقاوم است.
حتی برخی از قویترین تارهای عنکبوت نیز از جنس پلی آمید هستند. این تارها از نظر استحکام نسبی، از فولاد نیز قویتر هستند. طبیعت با استفاده از این پلیمرها، راهحلهای مهندسی فوقالعادهای برای چالشهای بقا ابداع کرده است. مطالعه این مواد طبیعی الهامبخش توسعه بسیاری از پلیمرهای مصنوعی امروزی بوده است.
آمینها؛ سنگ بنای ساخت پلی آمید
برای درک چگونگی تشکیل پلی آمیدها، ابتدا باید با اجزای سازنده آن آشنا شویم. آمینها دستهای از ترکیبات آلی هستند که نقش اساسی در سنتز پلی آمیدها ایفا میکنند. این ترکیبات از اتمهای کربن، هیدروژن و نیتروژن تشکیل شدهاند. وجود اتم نیتروژن در ساختار آمینها، خواص شیمیایی و فیزیکی ویژهای به آنها میبخشد که برای تشکیل پیوند آمیدی ضروری است.
آمینها را میتوان بر اساس تعداد اتمهای هیدروژن جایگزین شده در گروه آمونیاک دستهبندی کرد. این دستهبندی بر روی واکنشپذیری و خواص فیزیکی آنها تأثیر مستقیم میگذارد. سادهترین عضو این خانواده متیل آمین است که به عنوان یک الگوی پایه برای درک رفتار سایر آمینها عمل میکند. این ترکیبات میتوانند به عنوان باز عمل کنند و با اسیدها واکنش دهند.
اهمیت آمینها تنها محدود به آزمایشگاههای شیمی نیست. این ترکیبات در بسیاری از فرآیندهای بیولوژیکی نیز حضور دارند. آمینواسیدها که واحدهای سازنده پروتئینها هستند، حاوی گروه عاملی آمین میباشند. این موضوع نشاندهنده نقش حیاتی آمینها در تشکیل پلیمرهای طبیعی مانند پروتئینها و در نتیجه، پلی آمیدهای طبیعی است.
متیل آمین؛ ساده ترین آمین و دلیل بوی ماهی!
متیل آمین (CH₃NH₂) سادهترین عضو خانواده آمینها محسوب میشود. این ترکیب از یک گروه متیل (CH₃-) متصل به یک گروه آمین (NH₂) تشکیل شده است. متیل آمین در شرایط استاندارد به صورت گازی است و بوی تند و مشخصی شبیه به ماهی فاسد شده دارد. همین بو یکی از راههای شناسایی اولیه این ترکیب و مشتقات آن است.
بوی تند ماهی دقیقاً ناشی از وجود همین ترکیب و سایر آمینهای فرار است. هنگامی که بافتهای ماهی تجزیه میشوند، ترکیبات حاوی نیتروژن موجود در آنها به آمینهای فرار مانند متیل آمین و تری متیل آمین تبدیل میشوند. این ترکیبات با انتشار در هوا و تحریک گیرندههای بویایی، حس بویایی ما را تحریک میکنند و همان بوی آشنا را ایجاد مینمایند.
اگرچه این بو ممکن است ناخوشایند باشد، اما وجود متیل آمین بسیار مهم است. این ترکیب نه تنها یک مدل آموزشی عالی برای درک خواص آمینهاست، بلکه در صنایع مختلف نیز کاربرد دارد. از متیل آمین در تولید حشرهکشها، حلالها و به عنوان ماده اولیه در سنتز بسیاری از ترکیبات شیمیایی دیگر استفاده میشود.
خواص منحصر به فرد آمین ها به خاطر اتم نیتروژن
تمامی خواص ویژه آمینها به دلیل حضور اتم نیتروژن در ساختار آنهاست. این اتم دارای یک جفت الکترون ناپیوندی است که میتواند پروتون (H⁺) بپذیرد. این ویژگی باعث میشود آمینها خاصیت بازی از خود نشان دهند و بتوانند با اسیدها واکنش داده و نمک تولید کنند. این واکنشپذیری بالا، اساس تشکیل پیوند آمیدی است.
حضور اتم نیتروژن بر روی خواص فیزیکی آمینها نیز تأثیر میگذارد. این اتم میتواند پیوند هیدروژنی قوی با مولکولهای آب تشکیل دهد. به همین دلیل، آمینهای کوچک با زنجیره کوتاه معمولاً در آب حلالیت خوبی دارند. این خاصیت در شکل ۱۶ کتاب درسی به خوبی نشان داده شده است که میتوانید ساختار و نحوه ارتباط مولکولها را مشاهده کنید.
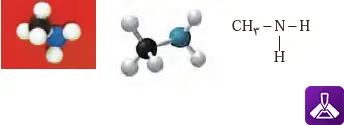
شکل 16 – فرمول ساختاری، مدل گلوله-میله و فضا پرکن متیل آمین
ویژگی دیگر آمینها، نقطه جوش نسبتاً بالاتر در مقایسه با ترکیبات آلی با وزن مولکولی مشابه است. دلیل این امر، امکان تشکیل پیوند هیدروژنی بین مولکولهای آمین است که انرژی بیشتری برای شکستن این پیوندها و تبخیر شدن ماده نیاز دارد. این خواص منحصر به فرد، آمینها را به ترکیباتی ایدهآل برای شرکت در واکنشهای پلیمری شدن تبدیل کرده است.
واکنش تشکیل پلی آمید؛ چگونه یک پلیمر قوی ساخته می شود؟
تشکیل پلی آمیدها یک نمونه کلاسیک از واکنش پلیمریزاسیون تراکمی است. این فرآیند بر پایه واکنش بین دو گروه عاملی کاملاً متفاوت اما مکمل استوار است. از یک سو گروه کربوکسیلیک اسید (COOH-) و از سوی دیگر گروه آمین (NH₂-) در این واکنش شرکت میکنند. حاصل این برهمکنش شیمیایی، ایجاد پیوندی محکم و آزاد شدن یک مولکول کوچک مانند آب است.
این واکنش نه تنها در آزمایشگاه، بلکه در بدن موجودات زنده نیز به طور مداوم در حال انجام است. زمانی که این فرآیند بین دو مولکول ساده انجام شود، یک دیمر یا اولیگومر تشکیل میدهد. اما وقتی بین مولکولهایی با دو گروه عاملی در هر طرف اتفاق بیفتد، زنجیرهای طولانی و مستحکم ایجاد میکند. این زنجیره طولانی همان پلیمر است که خواص فیزیکی و مکانیکی منحصر به فردی دارد.
استحکام نهایی پلی آمید حاصل به عوامل مختلفی بستگی دارد. طول زنجیره پلیمری، تعداد پیوندهای هیدروژنی بین زنجیرهها و آرایش فضایی مولکولها همگی در تعیین ویژگیهای نهایی محصول تأثیرگذار هستند. هرچه تعداد تکرار واحدهای سازنده در زنجیره بیشتر باشد، وزن مولکولی پلیمر بالاتر رفته و استحکام مکانیکی آن افزایش مییابد.
از واکنش اسید با آمین تا تشکیل پیوند آمیدی
واکنش بین یک اسید کربوکسیلیک و یک آمین، هسته اصلی تشکیل پیوند آمیدی است. در این واکنش، گروه هیدروکسیل (OH-) از اسید و یک اتم هیدروژن از گروه آمین جدا میشوند. این دو بخش با هم ترکیب شده و یک مولکول آب تشکیل میدهند. همزمان، بین کربن گروه کربونیل و نیتروژن گروه آمین، یک پیوند کووالانسی جدید تشکیل میشود.
این پیوند جدید که پیوند پپتیدی یا آمیدی نامیده میشود، یکی از مستحکمترین پیوندها در شیمی آلی است. دلیل این استحکام، رزونانس در گروه آمید است. جفت الکترونِ پیوند بین کربن و نیتروژن میتواند بین اتم کربن، اکسیژن و نیتروژن به اشتراک گذاشته شود. این پدیده باعث پایداری بیشتر پیوند و ایجاد ساختاری مسطح و سفت در گروه آمیدی میشود.
این واکنش به دما و کاتالیزور مناسب نیاز دارد. معمولاً برای پیشبرد واکنش به حرارت نیاز است تا مولکول آب حذف شده و تعادل واکنش به سمت تولید محصول پیش برود. در برخی موارد از کاتالیزورهای اسیدی یا بازی نیز برای تسریع واکنش استفاده میشود. این فرآیند دقیقاً مشابه واکنش تشکیل پلی استر است با این تفاوت که به جای گروه الکل، از آمین استفاده میشود.
تشریح واکنش پلیمری شدن پلی آمید
واکنش پلیمری شدن پلی آمید زمانی اتفاق میافتد که هر دو مونومر دارای دو گروه عاملی باشند. به عنوان مثال، یک دیآمین (با دو گروه NH₂) با یک دیاسید (با دو گروه COOH) واکنش میدهد. در مرحله اول، دو گروه عاملی با هم واکنش داده و یک دیمر با گروههای عاملی آزاد در دو انتها تشکیل میشود. این گروههای عاملی آزاد میتوانند با مونومرهای دیگر یا با دیمرهای دیگر واکنش دهند.
با ادامه واکنش، زنجیرهها به تدریج طولانیتر میشوند و پلیمر با وزن مولکولی بالا تشکیل میشود. این فرآیند را میتوانید در شکل ۱۷-الف کتاب مشاهده کنید. این شکل نشان میدهد چگونه یک پیوند آمیدی ساده تشکیل میشود.
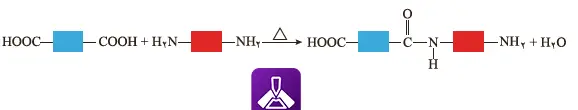
شکل 17-الف) تشكیل گروه آمیدی
اگر واکنش ادامه پیدا کند، گروههای آمیدی بیشتری تشکیل میشوند. در نهایت، این فرایند منجر به تولید پلی آمید میشود. مراحل این واکنش را در شکل 17-ب میتوانید بهخوبی مشاهده کنید.
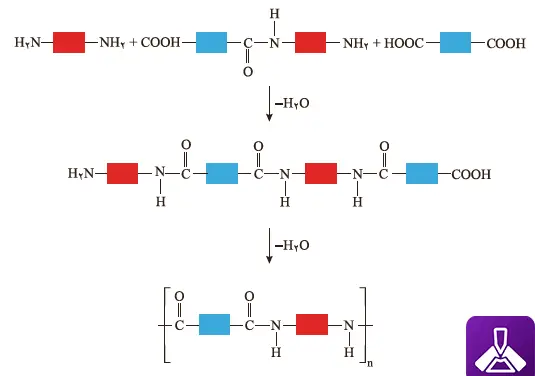
شکل 17-ب) الگوی واکنش تشکیل پلی آمید
در نهایت، زمانی که تعداد زیادی از این واحدهای تکرارشونده به هم متصل شوند، پلی آمید نهایی به دست میآید. هرچه درصد تبدیل گروههای عاملی بیشتر باشد، طول زنجیره پلیمری بیشتر و خواص مکانیکی بهتری خواهد داشت. کنترل شرایط واکنش مانند دما، زمان و نسبت مونومرها برای دستیابی به پلیمر با خواص مطلوب ضروری است.
کولار؛ معروف ترین پلی آمید مصنوعی و کاربردهای شگفت انگیز آن
کولار یک پلی آمید مصنوعی است که در صنایع پتروشیمی تولید میشود. این ماده از واکنش بین یک دی آمین و یک دی اسید به دست میآید. کولار به دلیل استحکام فوقالعاده بالا، به یکی از مهمترین مواد در صنایع مختلف تبدیل شده است. این پلیمر خاصیت منحصر به فردی دارد که آن را از سایر مواد متمایز میکند.
ویژگیهای کولار آن را به مادهای ایدهآل برای کاربردهای حساس تبدیل کرده است. این پلیمر در برابر حرارت، کشش و ضربه مقاومت بسیار بالایی از خود نشان میدهد. وزن سبک کولار در کنار استحکام بینظیرش، مزیت بزرگی محسوب میشود. این ترکیب خاصیتها، کولار را به انتخاب اول برای بسیاری از صنایع حساس تبدیل کرده است.
توسعه کولار انقلابی در صنایع ایمنی و حفاظتی ایجاد کرد. این ماده توانست مسیر جدیدی در تولید تجهیزات محافظتی پیشرفته باز کند. امروزه کولار نقش حیاتی در حفظ ایمنی و نجات جان انسانها در شرایط خطرناک ایفا میکند. این پلیمر تاکنون جان میلیونها انسان را در حوادث گوناگون نجات داده است.
روش تولید صنعتی کولار از دی آمین و دی اسید
تولید صنعتی کولار از طریق واکنش شیمیایی بین پارا-فنیلن دی آمین و ترفتالوئیل کلراید انجام میشود. این واکنش یک پلیمریزاسیون تراکمی است که در دمای کنترل شده صورت میگیرد. در این فرآیند، گروههای آمین و اسید با هم واکنش داده و پیوند آمیدی تشکیل میدهند. همزمان با تشکیل پیوند آمیدی، مولکولهای کوچکی مانند آب یا HCl آزاد میشوند.
فرآیند تولید شامل مراحل دقیق و کنترل شدهای است:
- اختلاط دقیق مونومرها در نسبتهای استوکیومتری
- انجام واکنش در دمای کنترل شده زیر نقطه ذوب پلیمر
- استفاده از حلالهای خاص برای تشکیل محلول پلیمری
- عملیات کشش الیاف برای همراستایی زنجیرههای پلیمری
محصول نهایی به صورت الیاف بسیار مستحکم به دست میآید. این الیاف سپس میتوانند به نخ تبدیل شده و در تولید منسوجات خاص مورد استفاده قرار گیرند. کنترل دقیق شرایط واکنش و پارامترهای فرآیند، تضمینکننده کیفیت نهایی محصول است.
چرا کولار اینقدر مقاوم است؟ (مقایسه با فولاد)
مقاومت استثنایی کولار به دلیل ساختار مولکولی منحصر به فرد آن است. زنجیرههای پلیمری کولار به صورت کاملاً منظم و موازی کنار هم قرار میگیرند. این آرایش منظم باعث تشکیل پیوندهای هیدروژنی قوی بین زنجیرهها میشود. پیوندهای هیدروژنی همراه با پیوندهای کووالانسی قوی در طول زنجیره، شبکهای بسیار مستحکم ایجاد میکنند.
در مقایسه با فولاد، کولار دارای مزایای قابل توجهی است:
- استحکام کششی پنج برابر بیشتر از فولاد هموزن
- وزن بسیار سبکتر نسبت به فولاد
- مقاومت در برابر خوردگی و مواد شیمیایی
- انعطافپذیری بالا همراه با استحکام
ساختار بلوری بالا و جهتگیری منظم زنجیرههای پلیمری، مهمترین عامل مقاومت کولار است. این ساختار باعث میشود انرژی ضربه در سراسر ماده توزیع شود. همچنین، پیوندهای آروماتیک در زنجیره پلیمری، پایداری حرارتی بالایی به کولار میبخشند.
کاربردهای کولار در زندگی و صنعت
کولار کاربردهای گسترده و متنوعی در صنایع مختلف پیدا کرده است. در صنایع نظامی و امنیتی، از کولار برای تولید جلیقههای ضد گلوله استفاده میشود. این جلیقهها با جذب و پراکنده کردن انرژی ضربه، از عبور گلوله جلوگیری میکنند. همچنین در کلاههای ایمنی و محافظهای بدنی نیز کاربرد دارد.
در صنعت حمل و نقل:
- تولید تایرهای مقاوم برای خودروها و هواپیماها
- ساخت بدنه قایقهای بادبانی و تجهیزات دریایی
- تولید قطعات سبکوزن در صنایع هوافضا
- ساخت ترمزهای صنعتی و کلاچهای با عملکرد بالا
در صنایع دیگر:
- تولید لباسهای ضد برش و ایمنی برای مشاغل پرخطر
- ساخت دستکشهای مقاوم در برابر بریدگی
- تولید طنابهای کموزن و مستحکم برای کوهنوردی
- عایقبندی کابلهای نوری و تجهیزات الکتریکی

شکل 18 – برخی کاربردهای کولار
همانطور که در شکل ۱۸ کتاب میبینید، کولار در تولید انواع محصولات ایمنی و صنعتی نقش حیاتی ایفا میکند. این پلیمر با ترکیب سبکی و استحکام فوقالعاده، امکان طراحی و تولید محصولاتی را فراهم کرده که پیش از این غیرممکن بود.
جمعبندی: پلیآمیدها؛ از پیوندهای مولکولی تا قهرمانی در زندگی روزمره
پلیآمیدها بهعنوان یکی از جذابترین موضوعات شیمی یازدهم، پیوند ناگسستنی بین مفاهیم پایه شیمی و کاربردهای پیشرفته صنعتی ایجاد میکنند. این ترکیبات نهتنها درک عمیقی از واکنشهای شیمیایی ارائه میدهند، بلکه اهمیت علم شیمی را در حل چالشهای واقعی زندگی نشان میدهند. از ساختار ساده متیلآمین تا پیچیدگیهای کولار، این مسیر آموزشی اهمیت یادگیری اصول شیمی را به خوبی نمایان میسازد.
ما در این مقاله به بررسی کامل پلیآمیدهای طبیعی و مصنوعی پرداختیم. پلیآمیدهای طبیعی مانند کراتین موجود در مو و ناخن، نشاندهنده هوشمندی طبیعت در طراحی مواد مستحکم هستند. از سوی دیگر، پلیآمیدهای مصنوعی مانند کولار، دستاورد بزرگ بشریت در تقلید از طبیعت و حتی پیشی گرفتن از آن محسوب میشوند. درک این مفاهیم نهتنها برای موفقیت در آزمونها، بلکه برای شناخت دنیای اطراف ما ضروری است.
مطالعه پلیآمیدها به خوبی نشان میدهد که چگونه یادگیری مفاهیم پایه شیمی میتواند به نوآوریهای شگفتانگیز منجر شود. از تولید جلیقههای ضدگلوله که جان انسانها را نجات میدهند تا ساخت تجهیزات پیشرفته صنعتی، همه و همه ریشه در درک همین مفاهیم شیمیایی دارند. این موضوع اهمیت تسلط بر فصل سوم شیمی یازدهم را به عنوان پایهای برای درک پیشرفتهتر علوم نشان میدهد.




برای ارسال نظر لطفا ابتدا وارد حساب کاربری خود شوید. صفحه ورود و ثبت نام