پلیمری شدن (بسپارش) چیست؟ – از مونومر تا پلیمر در شیمی یازدهم

احتمالاً همین حالا که در حال خواندن این مقاله هستید، یک کیسه پلاستیکی، یک بطری آب یا دستهی یک ظرف نچسب در اطرافتان وجود دارد. آیا تا به حال فکر کردهاید که این مواد متنوع و پرکاربرد از چه ساخته شدهاند؟ پاسخ این سؤال، به دنیای شگفتانگیز پلیمرها بازمیگردد.
یادگیری مفهوم پلیمری شدن یا بسپارش، که یکی از مباحث مهم و جذاب فصل سوم شیمی یازدهم است، به شما کمک میکند تا نه تنها در امتحانات موفق شوید، بلکه دنیای اطرافتان را بهتر درک کنید. این واکنش، فرآیندی است که در آن مولکولهای کوچک و ساده به هم متصل میشوند و مواد جدیدی با خواص کاملاً متفاوت و کاربردهای گسترده میسازند.
در این مقاله از سایت تدریس شیمی متین هوشیار، قصد داریم این مفهوم را به زبانی ساده و به صورت گام به گام، از پایه برای شما توضیح دهیم. ما به تمام سؤالات شما پاسخ خواهیم داد؛ از تعریف مونومر و پلیمر گرفته تا بررسی انواع ساختارهای پلیاتیلن و حل تمرینهای کتاب درسی. در پایان این مقاله، شما به طور کامل درک خواهید کرد که چگونه یک گاز ساده مانند اتن، به چنین محصولات متنوعی تبدیل میشود.
پلیمری شدن یا بسپارش چیست؟
پلیمری شدن یا بسپارش یکی از مهمترین فرآیندهای شیمیایی در صنعت و طبیعت است. در این واکنش، مولکولهای کوچک و ساده به نام مونومر (تکپار) به یکدیگر متصل میشوند و مولکولهای بسیار بزرگی با زنجیرههای طولانی به نام پلیمر (بسپار) میسازند. این فرآیند منجر به تولید موادی با خواص کاملاً جدید و کاربردهای گسترده میشود.
برای درک بهتر این مفهوم، میتوانید یک زنجیر بلند را تصور کنید که از اتصال حلقههای کوچک و یکسان به وجود آمده است. هر حلقه نماینده یک مونومر و زنجیر نهایی نماینده پلیمر است. این تغییر ساختار، باعث ایجاد مواد با استحکام بیشتر، انعطافپذیری متفاوت و مقاومت بالاتر در برابر حرارت و مواد شیمیایی میشود.
یک تعریف ساده و قابل درک
پلیمری شدن مانند ساختن یک قطار بلند از واگنهای یکشکل است. هر واگن به تنهایی کوچک و مستقل است اما وقتی به هم متصل میشوند، یک ساختار بزرگ و یکپارچه تشکیل میدهند. در دنیای شیمی، این واگنها مونومر نام دارند و قطار نهایی پلیمر نامیده میشود.
ویژگی اصلی این فرآیند، شکستن پیوندهای دوگانه در مونومرها و تشکیل پیوندهای جدید بین آنها است. این اتصال به صورت زنجیرهای ادامه پیدا میکند تا هزاران مونومر به هم متصل شوند. نتیجه نهایی، مادهای با جرم مولکولی بسیار بالا و خواص فیزیکی کاملاً متفاوت از مونومر اولیه است.
معادله واکنش پلیمری شدن اتن
واکنش پلیمری شدن اتن (اتیلن) نمونهای کلیدی و شناخته شده از این فرآیند است. در این واکنش، مولکولهای گازی اتن تحت شرایط خاصی به هم متصل میشوند و پلیاتن (پلیاتیلن) را تولید میکنند. معادله کلی این واکنش به صورت زیر نمایش داده میشود:
n(CH2=CH2) → (-CH2-CH2-)n
در این معادله:
- n تعداد مولکولهای اتن است که به هم متصل میشوند
- CH2=CH2 فرمول مولکولی مونومر اتن است
- (-CH2-CH2-)n فرمول ساختاری پلی اتن است
این واکنش در حضور کاتالیزور و تحت فشار و دمای کنترل شده انجام میشود. پیوند دوگانه بین اتمهای کربن در اتن شکسته میشود و هر اتم کربن میتواند با اتمهای کربن دیگر پیوند برقرار کند. به این ترتیب زنجیرههای طولانی پلیمری تشکیل میشوند.
مونومر و پلیمر؛ دو رکن اصلی بسپارش
مونومر و پلیمر دو مفهوم اساسی در فرآیند پلیمری شدن هستند که درک رابطه بین آنها برای فهم کامل بسپارش ضروری است. این دو مانند آجر و دیوار هستند؛ آجرهای کوچک و یکسان (مونومرها) در کنار هم قرار میگیرند و ساختاری بزرگ و مستحکم (پلیمر) میسازند. بدون مونومر، پلیمری تشکیل نمیشود و بدون پلیمر، مونومرها کاربرد عملی چندانی ندارند.
تفاوت اصلی بین مونومر و پلیمر در اندازه مولکولی و خواص فیزیکی آنهاست. مونومرها معمولاً مولکولهای کوچکی با جرم مولکولی پایین هستند که میتوانند به حالت گاز یا مایع وجود داشته باشند. در مقابل، پلیمرها مولکولهای غولپیکری با جرم مولکولی بسیار بالا هستند که اغلب به صورت جامدند و خواص مکانیکی منحصر به فردی نشان میدهند.
مونومر (تکپار) چیست؟
مونومر به مولکولهای کوچک و سادهای گفته میشود که میتوانند با اتصال به همدیگر، زنجیرههای پلیمری تشکیل دهند. واژه «مونومر» از دو بخش «مونو» به معنای تک و «مر» به معنای بخش تشکیل شده است. مونومرها واحدهای سازنده پلیمرها هستند و ویژگیهای ساختاری آنها تعیینکننده خواص نهایی پلیمر است.
ویژگیهای کلیدی مونومرها:
- دارای گروههای عاملی فعال برای ایجاد پیوند
- قابلیت تشکیل پیوند کووالانسی با سایر مونومرها
- داشتن پیوند دوگانه یا گروههای عاملی واکنشپذیر
- اندازه مولکولی کوچک و وزن مولکولی پایین
پلیمر (بسپار) چگونه تشکیل میشود؟
تشکیل پلیمر از طریق واکنش پلیمری شدن انجام میشود که در آن هزاران مونومر با ایجاد پیوندهای کووالانسی به هم متصل میشوند. این فرآیند میتواند به روشهای مختلفی انجام شود اما مکانیسم کلی شامل فعال شدن مونومرها و سپس اتصال متوالی آنها به یکدیگر است.
مراحل اصلی تشکیل پلیمر:
- آغاز واکنش: فعال شدن اولین مونومرها با کمک کاتالیزور یا آغازگر
- انتشار زنجیره: اتصال متوالی مونومرهای جدید به انتهای زنجیره در حال رشد
- پایان واکنش: توقف رشد زنجیره به دلایل مختلف مانند اتمام مونومر یا برخورد زنجیرهها
واحد تکرارشونده؛ کلید نوشتن فرمول پلیمرها
واحد تکرارشونده به بخشی از ساختار پلیمر گفته میشود که به صورت متوالی در طول زنجیره پلیمری تکرار میشود. این واحد در واقع همان بخشی از مونومر است که پس از تشکیل پیوند، در ساختار پلیمر باقی میماند. شناسایی واحد تکرارشونده کلید نوشتن فرمول صحیح پلیمرها است.
نحوه نمایش واحد تکرارشونده:
- در فرمولنویسی پلیمرها، واحد تکرارشونده داخل پرانتز قرار میگیرد
- زیروند «n» نشاندهنده تعداد تکرار این واحد در زنجیره است
- برای پلیاتن، واحد تکرارشونده (―CH₂―CH₂―) است
- فرمول پلیمر به صورت (―CH₂―CH₂―)n نمایش داده میشود
شناسایی واحد تکرارشونده به دانشآموزان کمک میکند تا بتوانند برای پلیمرهای مختلف فرمول بنویسند و رابطه بین ساختار مونومر و پلیمر را بهتر درک کنند. این مفهوم در حل بسیاری از مسائل شیمی پلیمر کاربرد دارد.
بررسی یک مثال کلیدی: پلی اتن (پلیاتیلن)
پلی اتن یا پلیاتیلن پرکاربردترین پلیمر مصنوعی در جهان است که به عنوان یک مثال عینی و ملموس از فرآیند پلیمری شدن مورد مطالعه قرار میگیرد. این پلیمر از پلیمریزاسیون مونومر اتن (اتیلن) به دست میآید و به دلیل خواص منحصر به فردش، در صنایع مختلف کاربردهای گستردهای دارد. تولید سالانه پلیاتیلن در جهان به دهها میلیون تن میرسد که نشاندهنده اهمیت اقتصادی و صنعتی این ماده است.
ویژگیهای فیزیکی و شیمیایی پلیاتن آن را به مادهای ایدهآل برای بسیاری از مصارف تبدیل کرده است. این پلیمر سبکوزن، مقاوم در برابر رطوبت، عایق الکتریکی خوب و در برابر بسیاری از مواد شیمیایی پایدار است. همچنین، پلیاتن به راحتی قالبگیری شده و به اشکال مختلف درمیآید که این ویژگی، زمینه را برای تولید محصولات گوناگون فراهم میکند.
از کیسه پلاستیکی تا لوله؛ کاربردهای پلی اتن
کاربردهای پلیاتن به قدری متنوع است که میتوان آن را در اکثر جنبههای زندگی روزمره مشاهده کرد. از بستهبندی مواد غذایی تا لوازم خانگی و از صنایع ساختمانی تا پزشکی، پلیاتن نقش مهمی ایفا میکند. این تنوع کاربرد ناشی از توانایی تولید پلیاتن با چگالیها و خواص مختلف است.
مهمترین کاربردهای پلیاتن شامل:
- صنعت بستهبندی: تولید کیسههای پلاستیکی، فیلمهای بستهبندی و بطریها
- صنایع ساختمانی: لولههای انتقال آب و گاز، عایقهای کابل و مخازن ذخیره
- کالاهای مصرفی: اسباببازی، ظروف آشپزخانه و لوازم ورزشی
- صنایع پزشکی: تولید ظروف استریل، پروتزها و بستهبندی داروها
تفاوت پلی اتن سبک (LDPE) و سنگین (HDPE)
تفاوت بین LDPE و HDPE به ساختار مولکولی و شرایط تولید آنها برمیگردد. پلیاتن سبک (Low-Density Polyethylene) دارای ساختار شاخهدار است در حالی که پلیاتن سنگین (High-Density Polyethylene) ساختار خطی و بدون شاخه دارد. این تفاوت ساختاری باعث ایجاد خواص فیزیکی متفاوت در این دو نوع پلیاتن میشود.
مقایسه ویژگیهای LDPE و HDPE:
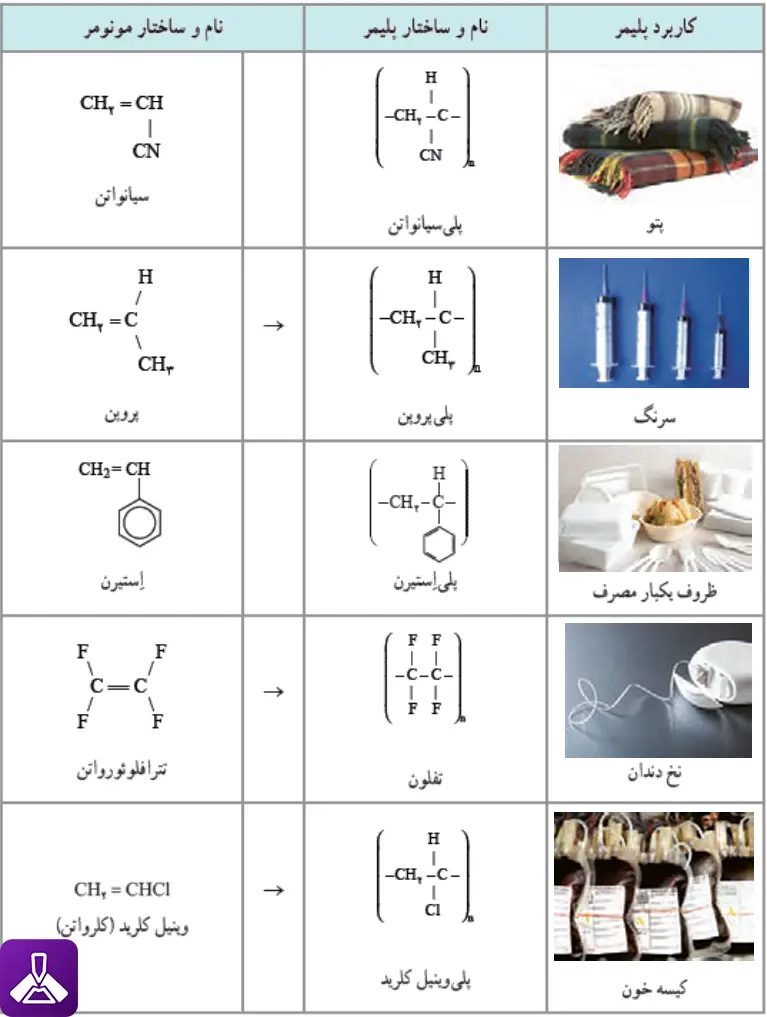
| ویژگی | پلیاتن سبک (LDPE) | پلیاتن سنگین (HDPE) |
|---|---|---|
| چگالی | ۰/۹۱-۰/۹۴ g/cm³ | ۰/۹۴-۰/۹۷ g/cm³ |
| درجه شفافیت | نیمهشفاف | کدر |
| انعطافپذیری | بالا | پایین |
| استحکام مکانیکی | پایین | بالا |
| دمای نرمشدن | ۸۵-۱۱۵°C | ۱۲۵-۱۳۵°C |
| کاربردهای اصلی | کیسههای پلاستیکی، فیلمها | لولهها، بطریها، مخازن |
این تفاوتها ناشی از نحوه اتصال مولکولهای مونومر به یکدیگر در طی فرآیند پلیمریزاسیون است. در LDPE، مولکولها به صورت تصادفی و با ایجاد شاخههای جانبی به هم متصل میشوند، در حالی که در HDPE اتصال به صورت منظم و بدون شاخههای جانبی انجام میشود.
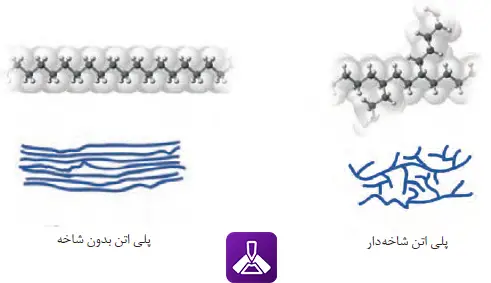
شکل 8- ساختار دو نوع پلی اتن
خود را بیازمایید صفحه 106 شیمی یازدهم
در جدول زیر هر یک از جاهای خالی را پر کنید.
جواب:
کشف تفلون؛ یک داستان جذاب علمی
کشف تفلون یکی از جذابترین داستانهای دنیای شیمی است که نشان میدهد چگونه یک مشاهده تصادفی در آزمایشگاه میتواند به یکی از بزرگترین اکتشافات علمی منجر شود. این کشف نه تنها در دنیای علم انقلابی ایجاد کرد، بلکه زندگی روزمره مردم را در سراسر جهان متحول ساخت. تفلون امروزه به عنوان نمادی از نوآوری و کاربردپذیری علم شیمی در صنعت شناخته میشود.
اهمیت این کشف تنها به خواص منحصر به فرد تفلون نیست، بلکه به رویکرد علمی محققان در بررسی یک پدیده غیرمنتظره بازمیگردد. این داستان به خوبی نشان میدهد که چگونه کنجکاوی علمی و پیگیری یک مشاهده به ظاهر کوچک میتواند به دستاوردهای بزرگ علمی بینجامد. تفلون امروزه در زمینههای مختلف از صنایع غذایی تا فناوری فضایی کاربرد دارد.
ماجرای کشف اتفاقی پلی تترافلوئورواتن (Teflon)
کشف اتفاقی تفلون در سال 1938 توسط دکتر روی پلانکت، شیمیدان آمریکایی، در آزمایشگاه شرکت دوپونت صورت گرفت. پلانکت در حال تحقیق بر روی گازهای خنککننده جدید بود و مشغول کار با گاز تترافلوئورواتن (TFE) شده بود. او قصد داشت با ذخیره کردن این گاز در سیلندرهای تحت فشار، خواص آن را بررسی کند.
رویدادهای منجر به کشف:
- پلانکت متوجه شد سیلندرهای حاوی گاز TFE به طور غیرمنتظرهای خالی شدهاند
- به جای گاز، پودر سفید رنگ جامدی در سیلندرها باقی مانده بود
- برخلاف انتظار، این ماده جامد نه تنها بیفایده نبود، بلکه خواص شگفتانگیزی داشت
- ماده جدید در برابر حرارت، مواد شیمیایی و سایش، مقاومت فوقالعادهای نشان میداد
این کشف کاملاً تصادفی بود اما پلانکت به جای نادیده گرفتن این پدیده، آن را به دقت بررسی کرد و فهمید که گاز TFE تحت فشار به پلیمری جامد به نام پلیتترافلوئورواتن (PTFE) تبدیل شده است. شرکت دوپونت این محصول را با نام تجاری «تفلون» به ثبت رساند.
خواص منحصر به فرد و کاربردهای تفلون
خواص استثنایی تفلون آن را به یکی از منحصر به فردترین مواد مهندسی تبدیل کرده است. این پلیمر دارای پایینترین ضریب اصطکاک در بین مواد جامد شناخته شده است و همین ویژگی آن را به مادهای ایدهآل برای کاربردهای غیرچسبنده تبدیل کرده است. همچنین مقاومت حرارتی بالایی دارد و تا دمای ۲۶۰ درجه سانتیگراد بدون تغییر باقی میماند.
مهمترین ویژگیهای تفلون:
- ضریب اصطکاک بسیار پایین (غیرچسبنده)
- مقاومت حرارتی بالا (تا ۲۶۰°C)
- مقاومت شیمیایی استثنایی در برابر اسیدها و بازها
- عایق الکتریکی عالی
- پایداری در برابر UV و آب و هوا
کاربردهای گسترده تفلون در صنایع مختلف:
- صنایع غذایی: پوشش ظروف نچسب مانند تابه و قابلمه
- صنایع شیمیایی: لولهها و شیرآلات مقاوم در برابر خوردگی
- صنایع الکترونیک: عایقکاری سیم و کابل
- صنایع پزشکی: ایمپلنتها و پروتزهای پزشکی
- صنایع نساجی: تولید پارچههای ضدلک و ضدآب
این خواص منحصر به فرد باعث شده تفلون به عنوان یکی از ارزشمندترین کشفیات علمی قرن بیستم شناخته شود و در زندگی روزمره میلیاردها نفر در سراسر جهان نقش ایفا کند.
خود را بیازمایید صفحه 109 شیمی یازدهم
داده های تجربی نشان می دهد که چگالی پلی اتن های نشان داده شده در شکل 8 برابر با 0/97 و 0/92 گرم بر سانتی متر مکعب است.
الف) کدام چگالی به کدام پلی اتن تعلق دارد؟ چرا؟
جواب: ۰/۹۲ چگالی پلیاتن شاخه دار و ۰/۹۷ چگالی پلیاتن بدون شاخه است. در پلیاتن شاخه دار به علت وجود شاخه، فاصله میان زنجیرها بیشتر بوده و جرم واحد آن کمتر است. به بیان دیگر در جرم برابر دو پلیمر، حجم پلی اتن شاخهدار بیشتر و چگالی آن کمتر است.
ب) کدام پلی اتن سبک و کدام سنگین است؟
جواب: پلیاتن شاخه دار، پلیاتن سبک و پلیاتن بدون شاخه، پلیاتن سنگین است.
پ) نیروی بین مولکولی در پلی اتن چیست؟
جواب: نیروی واندروالس
ت) چرا استحکام پلی اتن سنگین از سبک بیشتر است؟
جواب: زیرا با افزایش تعداد شاخه، مولکول ها به دلیل ازدحام فضایی نمیتوانند به هم نزدیک شوند، اما در پلیاتن که شاخه فرعی وجود ندارد سطح تماس مولکول ها بیشتر است و در نتیجه نیروی جاذبه بین مولکولی بیشتر شده و استحکام مولکولی هم بیشتر میشود.
جمعبندی نهایی: از مونومر تا دنیای شگفتانگیز پلیمرها
در این مقاله به طور کامل با مفهوم پلیمری شدن (بسپارش) به عنوان یکی از مباحث مهم فصل سوم شیمی یازدهم آشنا شدیم. یاد گرفتیم که این فرآیند، واکنشی شیمیایی است که در آن مولکولهای کوچک و ساده به نام مونومر (مانند اتن) در شرایط مناسب به یکدیگر متصل میشوند و مولکولهای بسیار بزرگی با زنجیرههای طولانی به نام پلیمر (مانند پلی اتن) تولید میکنند.
شما اکنون به خوبی میدانید که:
- مونومرها واحدهای سازنده و تکپارهای کوچکی هستند که قابلیت اتصال به هم را دارند.
- پلیمرها مواد جدیدی با خواص کاملاً متفاوت و کاربردهای بسیار گسترده هستند.
- واحد تکرارشونده کلید درک ساختار پلیمرها و نوشتن فرمول آنهاست.
- پلی اتن به دو شکل سبک (LDPE) و سنگین (HDPE) وجود دارد که هر کدام به دلیل تفاوت در ساختار مولکولی، خواص و کاربردهای متفاوتی دارند.
- کشف تفلون یک نمونه جذاب از نحوه پیگیری یک مشاهده تصادفی است که میتواند به نوآوریهای بزرگ منجر شود.
این مفاهیم نه تنها پایهای برای موفقیت در امتحانات هستند، بلکه به شما کمک میکنند تا دنیای اطراف خود را بهتر درک کنید. از کیسههای پلاستیکی تا ظروف نچسب، از لولههای انتقال آب تا قطعات الکترونیکی، همه و همه گوشهای از دنیای پهناور پلیمرها را به شما نشان میدهند.
امیدواریم این مقاله از سایت تدریس شیمی متین هوشیار توانسته باشد به شما در درک عمیقتر این مبحث کمک کند و اشتیاق شما را برای یادگیری بیشتر در دنیای شیمی افزایش دهد.




برای ارسال نظر لطفا ابتدا وارد حساب کاربری خود شوید. صفحه ورود و ثبت نام