تخریبپذیری یا ماندگاری پلیمرها؟ پاسخ را در ساختار مولکولی آنها بیابید

تفاوت سرنوشت پلیمرها در طبیعت، از تجزیه سریع یک پلیمر طبیعی تا ماندگاری یک پلاستیک برای قرنها، مستقیماً به معماری مولکولی و استحکام پیوندهای شیمیایی آنها وابسته است. این تمایز شیمیایی، پایهای برای درک یکی از مهمترین چالشهای زیست محیطی عصر حاضر و نیز مفاهیم پایهای در شیمی پلیمرها به شمار میرود.
این محتوای آموزشی، به تشریح بخشی از مباحث فصل سوم شیمی یازدهم اختصاص دارد و با هدف ارائه درکی عمیقتر از رابطهٔ ساختار و کارکرد پلیمرها طراحی شده است. ما در سایت تدریس شیمی متین هوشیار با بهرهگیری از شیوههای نوین آموزشی، قرار است این مفاهیم را برایتان سادهسازی کنیم.
در ادامه، فرآیند بنیادی آبکافت به عنوان کلید درک تخریب پلیمرها بررسی میشود. مکانیسم شکستن پیوندهای استری و آمیدی در پلیمرهای مصنوعی را تحلیل کرده و راز ماندگاری طولانیمدت پلیمرهای سیرشده را کشف میکنیم. در نهایت، راهکارهای علمی برای مدیریت پلیمرهای ماندگار از منظر شیمی را آموزش میدهیم.
نان شیرین میشود؟ نقطه آغاز درک تخریب پلیمرها
تجربهٔ سادهٔ جویده شدن نان در دهان و احساس طعم شیرین پس از چند دقیقه، یکی از ملموسترین مثالها برای درک مفهوم تخریب پلیمرها است. این پدیدهٔ روزمره، در واقع یک واکنش شیمیایی مهم را در مقیاس مولکولی نشان میدهد که پایهٔ درک رفتار پلیمرهای گوناگون در طبیعت است. بررسی این فرآیند، کلید فهم تفاوت بین پلیمرهای تخریبپذیر و ماندگار به شمار میرود.
نان و سیبزمینی از منابع غنی نشاسته هستند. نشاسته یک پلیمر طبیعی بزرگ و پیچیده است که از اتصال تعداد زیادی مونومر گلوکز ساخته شده است. این ساختار پلیمری در حالت عادی طعم شیرینی ندارد، اما زمانی که در معرض شرایط خاصی قرار می گیرد، شروع به تجزیه می کند.
داستان شیرین شدن نان در دهان، داستان شکسته شدن این پلیمر بزرگ به اجزای سازندهٔ آن است. این فرآیند که «آبکافت» نام دارد، نه تنها در دهان، بلکه در کل سیستم گوارشی و همچنین در محیط طبیعی برای پلیمرهای مختلف اتفاق میافتد. درک این مکانیسم، اولین گام برای پیشبینی سرنوشت یک پلیمر در محیط زیست است.
نشاسته؛ یک پلیمر طبیعی و تخریبپذیر
نشاسته یک پلیساکارید یا قند پیچیده است که به عنوان یک پلیمر طبیعی شناخته میشود. مونومرهای سازندهٔ این پلیمر، مولکولهای گلوکز هستند که با پیوندهای گلیکوزیدی به یکدیگر متصل شدهاند. این زنجیرهٔ طولانی پلیمری، در حالت عادی طعمی خنثی دارد و مزهٔ شیرین گلوکز در آن احساس نمیشود.
ویژگی کلیدی نشاسته به عنوان یک پلیمر تخریبپذیر، در ساختار شیمیایی آن نهفته است. پیوندهای گلیکوزیدی بین مولکولهای گلوکز، نسبت به حملهٔ مولکولهای آب آسیبپذیر هستند. این آسیبپذیری، امکان شکسته شدن زنجیره در شرایط مناسب را فراهم میکند که اساس فرآیند تخریب است.
تخریبپذیری نشاسته یک مزیت زیستی مهم است. موجودات زنده از جمله انسان، با استفاده از آنزیمهای خاصی این پیوندها را به سرعت میشکنند و گلوکز را که منبع انرژی است، آزاد میکنند. به همین دلیل است که نشاسته به عنوان یک پلیمر طبیعی و کاملاً تخریبپذیر در نظر گرفته میشود.
واکنش آبکافت: فرآیند کلیدی شکستن پیوندها
واکنش آبکافت یا هیدرولیز، یک واکنش شیمیایی بنیادی است که در طی آن یک پیوند شیمیایی با افزوده شدن یک مولکول آب شکسته میشود. در مورد پلیمرها، این واکنش باعث شکسته شدن پیوندهایی میشود که مونومرها را به هم متصل کردهاند و در نهایت پلیمر را به اجزای سازندهٔ خود تبدیل میکند.
در مثال نشاسته، واکنش آبکافت پیوندهای گلیکوزیدی را هدف قرار میدهد. یک مولکول آب به این پیوند حمله کرده و آن را میشکند که نتیجهٔ آن، آزاد شدن یک مولکول گلوکز است. تجمع این مولکولهای آزاد شدهٔ گلوکز است که طعم شیرین در دهان ایجاد میکند.
سرعت واکنش آبکافت میتواند بسیار کند باشد، اما به کمک کاتالیزگرها به طور چشمگیری افزایش مییابد. در دهان، آنزیمهای موجود در بزاق نقش کاتالیزگر را ایفا میکنند و فرآیند تجزیهٔ نشاسته را تسریع میکنند. این اصل برای تمام پلیمرهای تخریبپذیر صادق است؛ هرچه پیوندها مستعدتر و شرایط برای آبکافت مساعدتر باشد، سرعت تخریب پلیمر بیشتر خواهد بود.
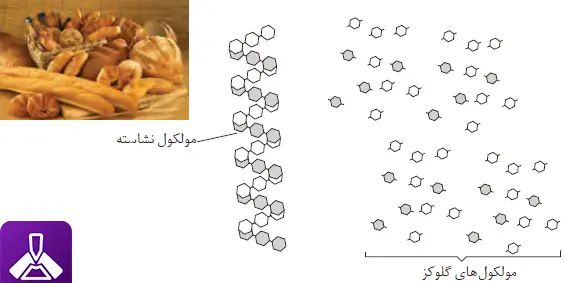
شکل 19 – الگوی تبدیل نشاسته به مونومرهای سازندۀ آن
تخریب پلیمرهای مصنوعی: از پیوند استری تا پیوند آمیدی
تخریب پلیمرهای مصنوعی نیز از همان قانون کلی حاکم بر نشاسته پیروی میکند، با این تفاوت که نوع پیوندهای شیمیایی و استحکام آنها سرنوشت نهایی پلیمر را تعیین میکند. پیوندهای استری و آمیدی که به ترتیب در پلیاسترها و نایلونها یافت میشوند، اگرچه مستعد آبکافت هستند، اما سرعت شکسته شدن آنها به شرایط محیطی بسیار وابسته است. این موضوع دلیل دوام بالای لباسهای پلیاستری و نایلونی در برابر تخریب را توضیح میدهد.
برخلاف پیوندهای موجود در نشاسته که به سرعت توسط آنزیمها شکسته میشوند، پیوندهای استری و آمیدی در پلیمرهای مصنوعی در برابر آبکافت مقاومت بیشتری نشان میدهند. این مقاومت ناشی از ساختار الکترونی و پایداری این پیوندها در شرایط عادی محیطی است. با این حال، در حضور کاتالیزگرهای مناسب مانند اسیدها، بازها یا آنزیمهای خاص، این پیوندها نیز میشکنند.
مطالعهٔ رفتار این پیوندها در برابر آبکافت نه تنها برای درک دوام پلیمرها، بلکه برای توسعهٔ راهکارهای مدیریت پسماندهای پلاستیکی نیز ضروری است. با درک دقیق مکانیسم آبکافت این پیوندها، میتوان پلیمرهایی طراحی کرد که پس از پایان عمر مفید خود، سریعتر و بیضررتر تجزیه شوند.
آبکافت استرها و پلیاسترها
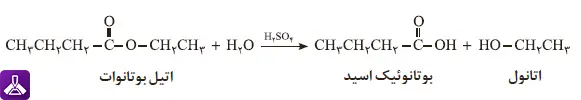
پیوند استری که مشخصهی استرها و پلیاسترها است، از واکنش بین یک گروه کربوکسیلیک اسید و یک گروه الکل تشکیل میشود. این پیوند میتواند در یک واکنش آبکافت و در حضور کاتالیزگر اسیدی یا بازی به اجزای سازندهٔ خود شکسته شود. یک نمونه کلیدی از این واکنش، آبکافت اتیل بوتانوات است که منجر به تولید اتانول و اسید بوتانوئیک میشود. این مثال ساده، الگویی برای درک رفتار پلیاسترها در برابر آب ارائه میدهد.
در پلیاسترها، این پیوند استری به صورت مکرر در طول زنجیرهٔ پلیمری وجود دارد. آبکافت پلیاسترها به معنای شکسته شدن همین پیوندها در سرتاسر زنجیره است که در نهایت منجر به تولید مونومرهای اولیه میشود. با این حال، به دلیل شرایطی مانند تبلور و فشردگی زنجیرههای پلیمری، دسترسی به این پیوندها برای مولکولهای آب محدود است و همین امر سرعت آبکافت را بسیار کند میکند.
به همین دلیل است که یک لباس پلیاستری میتواند برای سالها بدون تخریب قابل توجهی مورد استفاده قرار گیرد، مگر اینکه در معرض شرایط خاصی مانند محیطهای بسیار اسیدی، بازی یا دمای بالا قرار گیرد که سرعت آبکافت را افزایش میدهند. درک این مکانیسم برای دانش آموزان نشان میدهد که چگونه یک واکنش شیمیایی ساده در مقیاس کوچک (مانند اتیل بوتانوات) میتواند به درک رفتار مواد در مقیاس بزرگ (پلیاستر) کمک کند.
آبکافت پلیآمیدها (نایلون)
پلیآمیدها یا نایلونها دارای پیوند آمیدی هستند. این پیوند از واکنش بین یک گروه آمین و یک گروه کربوکسیلیک اسید تشکیل میشود. مکانیسم آبکافت پیوند آمیدی بسیار شبیه به پیوند استری است و در آن نیز یک مولکول آب وارد شده و پیوند را میشکند تا اسید کربوکسیلیک و آمین مربوطه را تولید کند.
اگرچه پیوند آمیدی نیز مستعد آبکافت است، اما به دلیل قدرت پیوند و همچنین اثرات فضایی در ساختار پلیمر، شکستن آن در شرایط عادی به کندی صورت میگیرد. نایلونها در برابر سایش و پارگی مقاوم هستند، اما در صورت قرارگیری طولانیمدت در معرض رطوبت و به ویژه رطوبت گرم، میتوانند دچار تخریب تدریجی شوند.
این ویژگی توضیح میدهد که چرا برخی از محصولات نایلونی در محیطهای مرطوب به مرور زمان استحکام خود را از دست میدهند. با این حال، در شرایط معمولی، سرعت این واکنش آنقدر کند است که نایلون به عنوان یک پلیمر بادوام در نظر گرفته میشود و تخریب آن میتواند دههها طول بکشد.
چرا برخی پلیمرها برای همیشه ماندگار میمانند؟
برخلاف پلیمرهای طبیعی مانند نشاسته یا پلیمرهای مصنوعی با پیوندهای مستعد مانند استر و آمید، برخی پلیمرها به گونهای طراحی شدهاند که در برابر فرآیند آبکافت مقاومت بسیار بالایی از خود نشان میدهند. این مقاومت، ناشی از ساختار شیمیایی خاص و نوع پیوندهای موجود در این پلیمرهاست که آنها را به موادی تقریباً جاودانه تبدیل کرده است. درک دلایل این ماندگاری طولانیمدت، کلید حل معضل آلودگی پلاستیکها در جهان است.
مقاومت در برابر تخریب، یک ویژگی ذاتی برای پلیمرهایی است که از زنجیرههای هیدروکربنی سیرشده و بدون گروههای عاملی حساس ساخته شدهاند. در این پلیمرها، پیوندهای کربن-کربن و کربن-هیدروژن بسیار پایدار و غیرفعال هستند و تمایل چندانی به واکنش با عوامل تخریبگر مانند آب، اکسیژن یا آنزیمها ندارند. این ویژگی، باعث میشود این مواد برای دههها یا حتی قرنها در محیط زیست بدون تغییر باقی بمانند.
این پایداری شیمیایی اگرچه از نظر کاربردی و اقتصادی مطلوب به نظر میرسد، اما از دیدگاه زیستمحیطی به یک چالش بزرگ تبدیل شده است. زیرا پس از پایان عمر مفید این محصولات، هیچ راهکار طبیعی برای بازگشت آنها به چرخهٔ طبیعت وجود ندارد و این مواد به صورت زبالههای تجزیهناپذیر انباشته میشوند.
ساختار مولکولی؛ تعیینکننده سرنوشت نهایی
ساختار مولکولی یک پلیمر، مهمترین عامل تعیینکنندهی سرنوشت نهایی آن در طبیعت است. پلیمرهای ماندگار مانند پلیاتیلن (PE) و پلیپروپیلن (PP) دارای ساختاری مشابه آلکانها هستند. در این پلیمرها، زنجیرههای کربنی طولانی و سیرشده وجود دارد که فاقد هرگونه گروه عاملی مستعد حمله هستند.
پیوندهای کربن-کربن در این پلیمرها بسیار قوی و غیرقطبی هستند. این پیوندها در برابر عوامل مخرب طبیعی مانند آب، نور خورشید و میکروارگانیسمها مقاومت بالایی نشان میدهند. از آنجایی که هیچ نقطهٔ حملهای برای شروع واکنش آبکافت یا اکسایش در این مولکولها وجود ندارد، فرآیند تخریب به شدت کند شده یا به طور کامل متوقف میشود.
این ویژگی ساختاری باعث میشود پلیمرهای ماندگار در شرایط عادی محیطی، هزاران سال بدون تجزیهی قابل توجه باقی بمانند. حتی در صورت شکسته شدن مکانیکی به قطعات کوچکتر (میکروپلاستیکها)، ساختار شیمیایی آنها تغییر چندانی نمیکند و همچنان در محیط باقی میمانند.
پیامدهای ماندگاری: چالش آلودگی پلاستیکها
ماندگاری طولانیمدت پلیمرها در طبیعت، پیامدهای زیستمحیطی شدیدی به همراه دارد. این مواد در محیطهای مختلف از جمله اقیانوسها، جنگلها و حتی مناطق قطبی انباشته میشوند و تعادل طبیعی این اکوسیستمها را برهم میزنند. حیوانات ممکن است این مواد را با غذا اشتباه گرفته و پس از بلع، دچار آسیبهای داخلی شدید شوند.
انباشته شدن پلاستیکها در طبیعت علاوه بر آلودگی بصری، باعث آلودگی خاک و آب نیز میشود. مواد شیمیایی موجود در این پلیمرها میتوانند به تدریج به خاک و آبهای زیرزمینی نفوذ کرده و سلامت انسان و دیگر موجودات زنده را به خطر بیندازند. تجزیهی بسیار کند این مواد همچنین منجر به تولید میکروپلاستیکها میشود که امروزه به یک نگرانی جهانی تبدیل شدهاند.
هزینههای اقتصادی مدیریت این آلودگی نیز بسیار سنگین است. جمعآوری، انتقال و دفن زبالههای پلاستیکی، هزینههای زیادی را به شهرداریها و دولتها تحمیل میکند. علاوه بر این، آسیبهای وارده به صنعت گردشگری و شیلات در اثر آلودگی پلاستیکی، خسارات اقتصادی بیشتری را به همراه دارد.
راهکارهای انسان برای مدیریت پلیمرهای ماندگار
مواجهه با چالش پلیمرهای ماندگار نیازمند توسعه راهکارهای عملی و هوشمندانه است. دانش شیمی به ما میآموزد که نمیتوانیم تنها با تکیه بر فرآیندهای طبیعی به مقابله با این معضل برویم، بلکه باید راهکارهای فعالانهای را برای مدیریت این مواد ارائه دهیم. این راهکارها بر دو محور اصلی استوار است: مدیریت پلیمرهای موجود در چرخه مصرف و توسعه جایگزینهای مناسب برای آینده.
- اولین راهکار، تمرکز بر مدیریت صحیح پلیمرهای ماندگاری است که هم اکنون تولید و مصرف میشوند. این امر مستلزم ایجاد سیستمهای کارآمد جمعآوری، جداسازی و پردازش این مواد است. در این زمینه، نشانهگذاری استاندارد محصولات پلیمری نقش کلیدی ایفا میکند، چرا که امکان شناسایی و جداسازی دقیق انواع پلیمرها را فراهم میسازد.
- راهکار دوم، سرمایهگذاری بر توسعه و تولید پلیمرهای زیستتخریبپذیر است. این پلیمرها به گونهای طراحی میشوند که پس از پایان عمر مفید خود، تحت شرایط طبیعی تجزیه شده و به مواد بیضرر تبدیل شوند. این رویکرد پیشگیرانه، در بلندمدت میتواند مشکل انباشت پلیمرهای ماندگار در طبیعت را به طور ریشهای حل کند.
بازیافت: شناسایی و جداسازی بر اساس کدها
بازیافت علمی و اصولی پلیمرها، نیازمند شناسایی دقیق نوع مواد اولیه است. برای تحقق این هدف، سیستم بینالمللی کدگذاری پلیمرها توسعه یافته که در آن هر نوع پلیمر با عددی خاص داخل یک مثلث شناسایی میشود. این اعداد از 1 تا 7 بوده و هر کدام نشاندهنده نوع خاصی از پلیمرها هستند.
فرآیند بازیافت با شناسایی این کدها آغاز میشود. برای مثال، عدد 1 نشاندهنده پلیاتیلن ترفتالات (PET) و عدد 2 نشاندهنده پلیاتیلن با چگالی بالا (HDPE) است. این شناسایی دقیق امکان جداسازی صحیح پلیمرها را فراهم کرده و کیفیت محصولات بازیافتی را بهطور قابل توجهی افزایش میدهد.
استفاده از این سیستم کدگذاری در ایران نیز به صورت فزایندهای در حال گسترش است. انتظار میرود با نهادینه شدن فرهنگ استفاده از این نشانهها روی کلیه محصولات پلیمری، فرآیند بازیافت در کشور به صورت علمیتر و کارآمدتر انجام پذیرد. این امر نه تنها به حفظ محیط زیست کمک میکند، بلکه از نظر اقتصادی نیز به صرفه خواهد بود.
جایگزینی: عصر پلیمرهای زیستتخریبپذیر
جایگزینی پلیمرهای ماندگار با انواع زیستتخریبپذیر، یکی از امیدوارکنندهترین راهکارهای مقابله با آلودگی پلاستیکی است. این پلیمرها به گونهای طراحی میشوند که پس از مصرف، توسط میکروارگانیسمهای موجود در طبیعت به موادی بیضرر مانند آب، دیاکسید کربن و زیستتوده تبدیل شوند.
پلیمرهای زیستتخریبپذیر به دو دسته اصلی تقسیم میشوند: دسته اول پلیمرهای با منشأ طبیعی مانند پلیساکاریدها (نشاسته، سلولز) و پروتئینها هستند. دسته دوم پلیمرهای سنتزی هستند که به گونهای طراحی شدهاند که قابلیت تخریب پذیری داشته باشند. هر دو دسته این پلیمرها میتوانند در تولید انواع محصولات از کیسههای خرید تا بستهبندیهای مواد غذایی مورد استفاده قرار گیرند.
توسعه و استفاده از پلیمرهای زیستتخریبپذیر در دو دهه اخیر مورد توجه جهانی قرار گرفته است. سرمایهگذاری در این حوزه نه تنها باعث کاهش آلودگی محیط زیست میشود، بلکه میتواند فرصتهای اقتصادی جدیدی را نیز ایجاد کند. این راهکار، نشاندهنده تعادل بین پیشرفت صنعتی و حفظ محیط زیست است.
خود را بیازمایید صفحه 119 و 120 شیمی یازدهم
در این قسمت به بررسی و جواب سوالات خود را بیازمایید «پلیمرها، ماندگار یا تخریب پذیر» میپردازیم.
سوال 1)
در كدام شرایط زیر لباسهای نخی زودتر پوسیده میشوند؟ چرا؟
الف) محیط سرد و خشک
ب) محیط گرم و مرطوب
جواب: محیط گرم و مرطوب، زیرا پلی آمیدها و پلی استر در محیط گرم و مرطوب با آب واکنش میدهند و به مونومرهای سازنده تبدیل میشوند. با شکستن این پیوندها، استحکام الیاف پارچه کم شده و تار و پود آن به سادگی گسسته میشود.
سوال 2)
چرا استفادهی بی رویه از شویندهها در شستن لباسها سبب پوسیده شدن سریعتر آنها میشود؟
جواب: مواد موجود در شویندهها میتوانند سرعت آبکافت پلیاسترها یا پلی آمید الیاف پارچه را افزایش دهند. در نتیجه، سرعت شکسته شدن پیوندها در پلیمرهای سازندە لباس را بیشتر کنند. در چنین شرایطی سرعت پوسیده شدن پارچه نیز افزایش مییاید.
سوال 3)
اگر لباسها را برای مدت طولانی در محلول آب و شوینده قرار دهید، بوی بد و نافذی پیدا میکنند. توضیح دهید چه رخ میدهد؟
جواب: در این حالت شرایط مناسبی برای آبکافت پلیمر سازندە الیاف لباس و شکسته شدن آن به مونومرها ایجاد میشود و بوی حاصل به دلیل تولید مونومرهای اولیه یعنی اسید و الکل سازندە استر الیاف است.
سوال 4)
برای شستن تمیزتر لباسها از شویندهها و سفیدکنندهها استفاده میکنند. اگر سفید کنندهها را به طور مستقیم روی لباس بریزند، رنگ لباس در محل تماس به سرعت از بین میرود. اما اگر سفیدکننده را در آب بریزید سپس لباس را درون محلول فرو ببرید، تغییر محسوسی در رنگ لباس ایجاد نمیشود. چرا؟
جواب: هنگامی که سفید کننده مستقیماً روی لباس ریخته میشود، بهدلیل غلظت بالای آن سرعت واکنش بیشتر است در نتیجه به سرعت اثر آن ظاهر میشود. اما ریختن در آب، سبب رقیق شدن و کاهش غلظت آن شده و سرعت واکنش کاهش مییابد.
سوال 5)
لباسهای پلی استری در اثر عوامل محیطی در طول زمان پوسیده میشوند. این پوسیده شدن به معنی شکستن پیوندهای استری و سست شدن تار و پود لباس است. جدول زیر دادههای مربوط به واکنش آبکافت یک نوع استر را در حضور اسید نشان میدهد. با توجه به آن به پرسشهای مطرح شده پاسخ دهید:
| [استر] | 0/55 | 0/42 | 0/31 | 0/23 | 0/17 | 0/12 | 0/08 |
| زمان (s) | 0 | 15 | 30 | 45 | 60 | 75 | 90 |
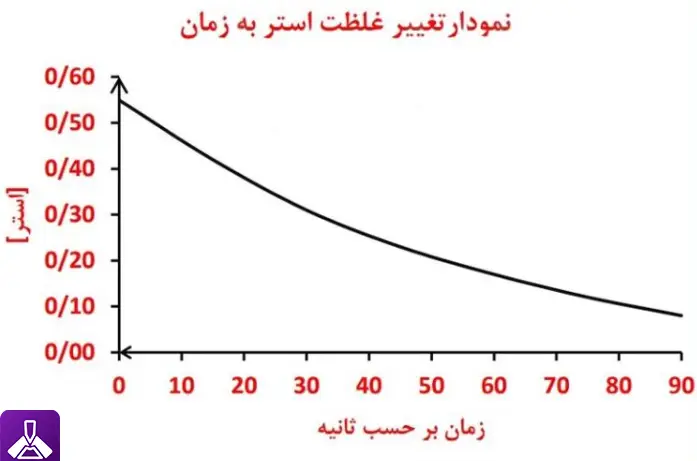
الف) نمودار تغییر غلظت استر بر حسب زمان را رسم کنید.
جواب:
ب) سرعت متوسط آبکافت استر در بازهی زمانی صفر تا 30 ثانیه چند مول بر لیتر بر ثانیه است؟
جواب:
پ) سرعت واکنش در کدام بازه زمانی بیشتر است؟ چرا؟
- صفر تا 20 ثانیه
- 60 تا 90 ثانیه
جواب: سرعت واکنش در بازه صفر تا ٢٠ ثانیه بیشتر است زيرا در آغاز واكنش، غلظت استر بیشتر است و مقدار بیشتری از آن آبکافت میشود. به عبارت دیگر، در آغاز واکنش شیب نمودار تجزیه استر بیشتر است و با گذشت زمان و کاهش غلظت استر، سرعت آبکافت آن کاهش خواهد یافت.
جمعبندی: از شناخت مولکولها تا انتخاب مسئولانه
مطالعه پلیمرها به ما میآموزد که ساختار مولکولی، تعیینکننده سرنوشت نهایی مواد در طبیعت است. همانطور که پیوندهای مستعد آبکافت در نشاسته و پلیاسترها امکان تخریب را فراهم میکنند، پیوندهای پایدار کربن-کربن در پلیاولفینها ماندگاری طولانیمدت ایجاد میکنند.
در حال حاضر با دو راهکار اصلی میتوان با چالش پلیمرهای ماندگار مقابله کرد:
🔄 بازیافت هوشمندانه با استفاده از سیستم کدگذاری استاندارد
🌱 جایگزینی با پلیمرهای زیستتخریبپذیر
این مقاله به شما نشان داد که چگونه درک مفاهیم شیمی میتواند به انتخابهای آگاهانهتر و مسئولانهتر منجر شود. هر دانشآموز میتواند با شناخت دقیقتر پیوندهای شیمیایی، نقش خود را در حفاظت از محیط زیست به خوبی ایفا کند.
به یاد داشته باشید: انتخاب مواد تنها یک تصمیم اقتصادی نیست، بلکه یک انتخاب زیستمحیطی با پیامدهای بلندمدت است. با به کارگیری دانش شیمی میتوانیم مسیر توسعه پایدار را هموار کنیم.

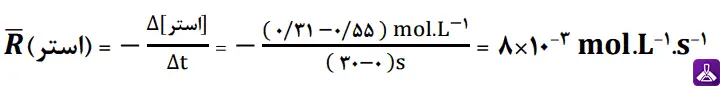



برای ارسال نظر لطفا ابتدا وارد حساب کاربری خود شوید. صفحه ورود و ثبت نام